מדוע גוף האדם פועל כנגד עצמו במחלות כמו סרטן? מחלות אוטואימוניות הן קבוצה של הפרעות כרוניות בהן מערכת החיסון של הגוף תוקפת בטעות תאים בריאים. כתוצאה מכך, מתרחשת דלקת וכאב ברקמות בריאות. זו גוררת לעיתים פגיעה קשה באיברים ובמערכות בגוף עד כדי מוות. הסיבות המדויקות למחלות אוטואימוניות אינן ידועות. ואולם אך מחקרים מדעיים מצביעים על שילוב של גורמים גנטיים, סביבתיים ואימונולוגיים. ורמים גנטיים: מחקרים מצאו קשר בין נטייה גנטית לבין התפתחות מחלות אוטואימוניות. אם לאדם יש קרוב משפחה עם מחלה אוטואימונית, הסיכון שלו לחלות במחלה דומה עולה. עם זאת, קיום נטייה גנטית אינו מבטיח התפתחות של מחלה, וגורמים נוספים נדרשים. לצד זה משפיעים גם גורמים סביבתיים: חשיפה לגורמים סביבתיים מסוימים, כמו זיהומים, וירוסים, חיידקים, רעלים וחומרים כימיים, משפיעה לעתים על התפתחות מחלות אוטואימוניות אצל אנשים עם נטייה גנטית. מעבר לכך, גם גורמים אימונולוגיים משפיעים: פגמים במערכת החיסון, כמו תפקוד לקוי של תאי T רגולטוריים, יכולים להוביל לתגובה חיסונית לא תקינה כנגד רקמות בריאות.
מחקרים עדכניים מצביעים על כיווני זיהוי ופתרון של הסיבה לכך. חוקרים משתמשים בטכנולוגיות גנומיות חדשות כדי לזהות גנים ספציפיים הקשורים למחלות אוטואימוניות. זיהוי גנים אלה עשוי לסייע בפיתוח תרופות חדשות וטיפולים יעילים יותר. לצד זה גם מחקר מיקרוביום של חיידקי המעי מספק מענה מסוים לסוגיה: מחקרים חדשים מצביעים על קשר בין מערכת העיכול, המיקרוביום (החיידקים ה"טובים") שחיים בו, לבין התפתחות מחלות אוטואימוניות. שינויים במיקרוביום עשויים להשפיע על מערכת החיסון ועל הסיכון למחלות אלה. לצד זה בחזית הטיפולית גם טיפולים חדשים, כמו טיפולי CAR-T, מכוונים לחיזוק מערכת החיסון ותקיפת תאים פגועים הגורמים למחלות אוטואימוניות.
גורמים רבים תורמים להתפתחות מחלות אוטואימוניות, ביניהם גורמים גנטיים, סביבתיים ואימונולוגיים. מחקרים מדעיים מתקדמים ממשיכים לחקור את הגורמים הללו במטרה לפתח תרופות וטיפולים יעילים יותר למחלות אלו. ממצאים ייחודיים שפורסמו על ידי מדענים ממכון וייצמן מנסים גם הם לגלות מדוע תוקפת המערכת החיסונית את גופנו. מודל חדש מסביר מדוע המערכת החיסונית תוקפת את רקמות הגוף ומה גורם למחלות אוטואימוניות כמו סוכרת, זאבת או סרטן.
לפי מודל חדש שפיתחו מדעני מכון ויצמן ייתכן שמחלות אוטואימונית אינן מקרה של טעות בזיהוי הגורמת למערכת החיסונית להתקיף רקמות בריאות במקום פולשים מבחוץ. לפי מודל זה ייתכן שמדובר דווקא בפעילות תקינה של המערכת החיסונית נגד "איומים מבפנים". מדובר בעצם בפעילות אשר במקרים מסוימים יוצאת מכלל שליטה. המודל החדש מציע גם פתרון לחידה ארוכת שנים: מדוע איברים מסוימים בגוף חשופים למחלות אוטואימוניות יותר מאחרים? הממצאים מתפרסמים היום בכתב-העת המדעי Immunity.
מחלות אוטואימוניות נחלקות לשני סוגים – מחלות מערכתיות, כמו זאבת, שתוקפות איברים רבים בגוף, ומחלות כגון סוכרת מסוג 1 (סוכרת נעורים), המשפיעות על איבר יחיד. מסבירה יעל כורם-כהנים, תלמידת מחקר במעבדתו של פרופ' אורי אלון במחלקה לביולוגיה מולקולרית של התא, שהובילה את המחקר, אחת השאלות הפתוחות לגבי סוג המחלות השני, היא מדוע איברים או תאים מסוימים חשופים למחלות אוטואימוניות – בעוד אחרים כמעט כלל לא. המחקר של כורם-כהנים נערך בהשתתפות תלמיד המחקר אביחי טנדלר ומדען הסגל ד"ר אבי מאיו מקבוצתו של פרופ' אלון, בשיתוף פעולה עם קבוצת המחקר של פרופ' ניר פרידמן מהמחלקה לאימונולוגיה.
אחת הדוגמאות לכך היא הלבלב. בלבלב תאי הבטא מייצרי האינסולין נפגעים בשיעורים גבוהים כתוצאה ממחלות אוטואימוניות. ואולם הם מהווים רק 2%-4% מתאי הלבלב, בעוד יתר תאיו כמעט שאינם מעורבים במחלות אלה. בדומה לכך, מחלת הַשימוֹטוֹ משפיעה על בלוטת התריס של כ-7% מהאוכלוסייה. זאת בעוד שבלוטת יותרת התריס הסמוכה אליה כמעט שאינה נפגעת ממחלה אוטואימונית כזו. מה שמשותף למחלות אלה הוא שהמחלות הללו מופיעות לראשונה בילדים או במבוגרים צעירים. זאת בניגוד למחלות גנטיות המופיעות כבר בלידה או למחלות זקנה – והן כרוכות באופן ספציפי בהרס תאים המפרישים הורמונים חיוניים (תאים אנדוקריניים). במלים אחרות, נראה כאילו ביום בהיר אחד באמצע החיים, תאי T של המערכת החיסונית מסמנים את התאים האנדוקריניים כאיום ומחסלים אותם.
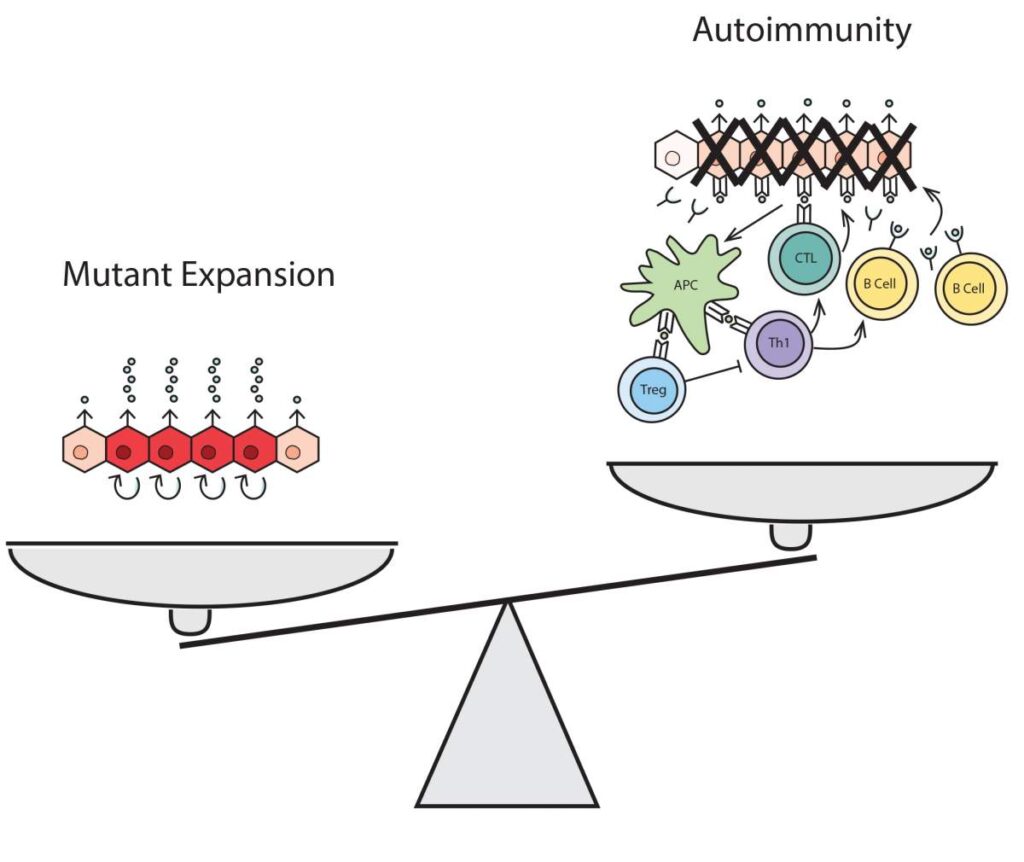
נקודת המוצא של המחקר הייתה שאולי תאי T נועדו מלכתחילה לחסל תאים אלה? הורמונים כמו אינסולין, הורמוני בלוטת התריס וקורטיזול, נוטים לפעול ב"לולאות משוב": כשהביקוש להורמון עולה, התאים יגבירו לא רק את ייצור ההורמון ואת הפרשתו, אלא גם את קצב החלוקה שלהם – במטרה לעמוד בביקושים לאורך זמן. התחלקות התאים טומנת בחובה סיכונים: בשיעור מסוים מהתאים החדשים יופיעו מוטציות. מרבית המוטציות הן בלתי-מזיקות, אך כשהמוטציה משבשת את מכונות החישה העדינות של התא – התא עלול לפרש דרישה נמוכה להורמון כדרישה גבוהה. שגיאה שכזאת היא קטלנית: התא לא רק ימשיך להפריש עוד ועוד מההורמון, הוא גם יתחלק שוב ושוב וכך ייצר תאים חדשים עם אותה המוטציה, שבתורם, יתחלקו שוב ושוב וייצרו עוד ועוד מההורמון. התוצאה: פגיעה קשה בגוף.
בהתאם למודל שהמדענים פיתחו תאי המערכת החיסונית מסוג T מספקים בשגרה שכבת הגנה שנועדה להבטיח כי רמות ההורמונים בגוף יהיו תחת בקרה. למעשה, אפשר לומר שהם אמונים על סיכול "טרור פנימי": תאי T פועלים כסוכנים חשאיים המסלקים תאים אנדוקריניים אשר מאיימים להשתלט על איבר מסוים ולהפריש כמויות גבוהות מדי של הורמון שיביאו לסכנת חיים אם לא ייעצרו בזמן. במחלות אוטואימוניות, תאי T המוכוונים לביצוע משימה זו עשויים להפוך לנלהבים יתר על המידה ולחסל גם תאים בריאים. במלים אחרות, מחלות אוטואימוניות הן תוצאה של שכבת בקרה שנועדה למנוע מחלות שקשורות בייצור עודף של הורמונים, תוך סיכון לתוצאה הפוכה אצל אנשים מסוימים – ייצור מופחת.
יחד עם זאת לא ברור למה בלוטות מסוימות אינן נפגעות ממחלות אוטואימוניות? האם בלטות אלה "ויתרו" על ההגנה של תאי T? בלוטת יותרת התריס, לדוגמה, אמנם לא נוטה להיפגע ממחלות אוטואימוניות. ואולם היא נוטה מאוד לגידולים לא-סרטניים הנקראים אדנומות ונפוצים בקרב נשים בגיל המעבר. האדנומות מפרישות כמויות אדירות של הורמון, הגורמות לפעילות יתר מזיקה של בלוטת יותרת התריס (hyperparathyroidism). דוגמאות אחרות, אף שהן דרמטיות פחות מזו של בלוטת יותרת התריס, נתנו אף הן תמיכה לרעיון שהיעדר התערבותם של תאי T, אכן עלול לגרום להפרשת הורמונים מוגברת ולחלוקת תאים בלתי-מבוקרת.
כורם-כהנים מציינת כי "המודל מאפשר להסביר כמה ממצאים תמוהים. לדוגמה, בדקנו רצפים גנטיים של תאי T שנמצאו אצל אנשים בריאים, וראינו כי לחלק מהתאים יש בדיוק את אותם קולטנים מזהי-חלבון כמו בתאי T מחולים במחלות אוטואימוניות. ההסבר המקובל לכך הוא שאנשים בריאים לוקים בגרסה קלה של המחלה, או במחלה בשלביה המוקדמים. אך הגיוני יותר להניח שתאי T אלה אמורים להיות שם; הם נועדו למנוע חלוקת תאים עודפת וייצור עודף של הורמונים". כורם-כהנים אומרת עוד שהמודל מציע פתרון לחידה שהעסיקה חוקרים זמן רב, אך יש צורך לבצע ניסויים כדי לבחון אם התחזיות מתממשות בפועל.
עם זאת, כבר כיום המודל מעורר עניין ועומד במוקד הדיון בקרב אימונולוגים מובילים. החוקרים מהמעבדה של פרופ' אלון ממשיכים לעבוד יחד עם הקבוצה של פרופ' פרידמן על אמצעים לבחינת תוצאות המודל באופן ניסיוני.
פרופ' אלון מציין כי "אנחנו סבורים שמחלות אוטואימוניות אינן מגיעות משום-מקום. כן, זוהי תקלה, אך זו תקלה במערכת פיסיולוגית תקינה ופועלת. אנו צועדים בעקבות עבודותיהם החלוציות של פרופ' ירון כהן ופרופ' מיכל שוורץ ותלמידיהם ממכון ויצמן למדע, שהדגישו את הדואליות של המערכת החיסונית אשר בו-בזמן אמונה הן על טיפול בגופנו והן על מלחמה בפולשים מבחוץ".